近日,迪安診斷凱萊譜實驗室與溫州市中心醫院、西湖大學等單位合作,對新冠長病程和短病程患者代謝組學和蛋白質組學多組學聯合分析的成果在線發表于Cell Discovery雜志(影響因子38.079)。凱萊譜康洲陽博士是該文章的共同第一作者,孔子青博士是本文的共同通訊作者,迪安診斷凱萊譜實驗室和浙江省數字醫學診斷技術重點實驗室是共同作者單位。

前期,該研究團隊對新冠患者進行蛋白組和代謝組學橫斷面研究,發現新冠重癥患者血清中多種獨特的分子變化,并找到了一系列生物標志物(22種蛋白質、7種代謝物,涉及到體內巨噬細胞、血小板、補體系統的代謝通路)用于預測輕癥患者向重癥發展過程[1];而通過尿液蛋白組和代謝組學發現由新冠引起的免疫紊亂會觸發炎癥反應、凝血反應以及細胞纖維化會最終損傷腎組織[2]。
為探究部分COVID-19患者表現出長時間的SARS-CoV-2感染持續陽性的原因,本研究基于縱向隊列,從病毒載量、免疫抗體水平、蛋白質組和代謝組學4個維度對長病程(LC)和短病程(SC)的COVID-19患者開展了相關研究,總計從461份血清樣本中鑒定到1252個蛋白和945個代謝物,全面揭示了新冠長病程患者的特異性機體代謝變化。
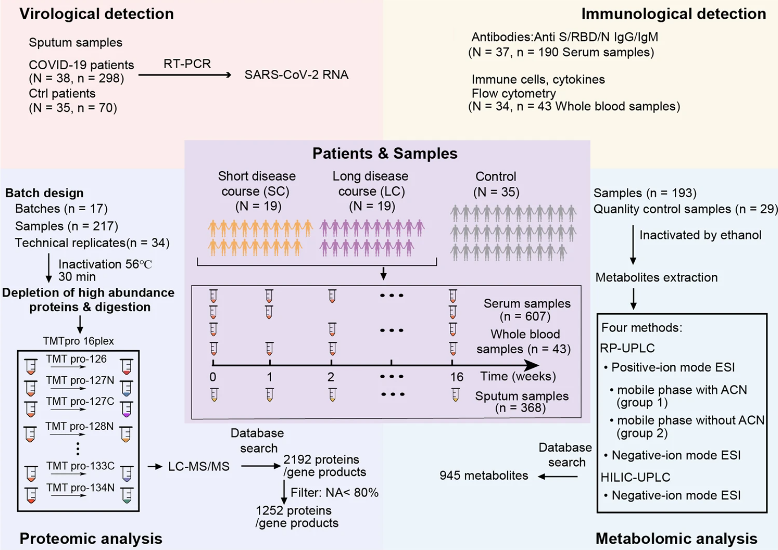
圖1 多組學實驗設計思路
研究首先發現LC和SC組患者在病毒載量方面并無顯著差異,而免疫學分析發現LC組患者表現出更長時間的高水平IgG抗體和更高的調節性T (Treg)細胞。對患者血清進行縱向蛋白質組學和代謝組學分析發現,病毒RNA脫落周期延長與肝臟X受體/視黃素X受體(LXR/RXR)通路抑制、多種抗炎代謝物(脂肪酸、EPA、DHA、癸酸、辛酸等)受到抑制、補體系統激活、細胞遷移抑制和病毒復制增強有關。對持續性病毒RNA脫落的評估是追蹤嚴重病毒感染的恢復和長期反應的一種方法。持續病毒脫落的檢測受初始疾病嚴重程度、病毒載量和樣本來源的影響。此外,利用機器學習方法成功建立預測模型(包括9種蛋白質NRP2, H3-3A, GNPTG, LGALS1, IGKV2-30, HLA-B, PRSS1, IGKV1-6, KPRP與1種代謝物arginine),可以預測新冠患者病毒RNA的脫落周期。
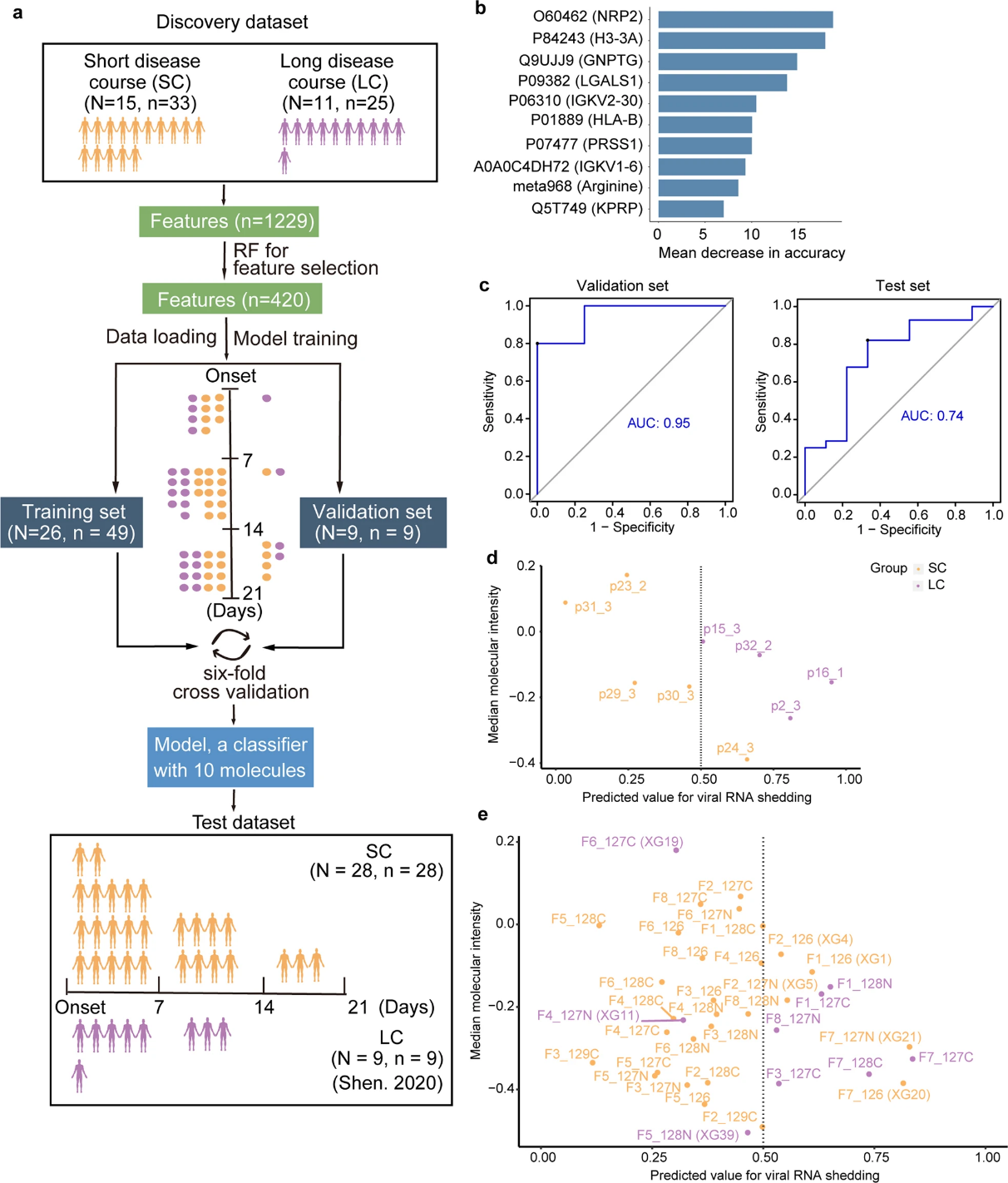
圖2 新冠病毒RNA脫落周期多組學評估模型
通過上述結果我們發現,相對于短病程患者,長病程的COVID-19患者表現出了明顯的炎癥增強和適應性免疫抑制。基于長病程患者特征性的蛋白和代謝變化,該研究成功建立了一種預測病毒RNA脫落周期的多組學評估模型。本研究填補了對新冠病毒RNA脫落機制研究的不足,對于幫助制定更好的策略來控制病毒的傳播至關重要,也為目前廣受關注的long-COVID研究提供了重要的理論基礎 [3]。
迪安診斷凱萊譜實驗室利用非靶向和靶向代謝組學技術以及多組學聯合分析平臺,連續3年在Cell、Cell Reports、Cell Discovery等頂級期刊分別從不同維度闡述了新冠病毒對人體免疫代謝系統的影響,持續為基于臨床質譜的疾病檢測和診斷、發生和發展、預防和治療提供理論和轉化應用研究基礎。
參考文獻:
1 Shen, Bo, et al. "Proteomic and metabolomic characterization of COVID-19 patient sera." Cell 182.1 (2020): 59-72.
2 Bi, Xiaojie, et al. "Proteomic and metabolomic profiling of urine uncovers immune responses in patients with COVID-19." Cell reports 38.3 (2022): 110271.
3 Crook, Harry, et al. “Long covid-mechanisms, risk factors, and management.” BMJ (Clinical research ed.) 374 (2021): n1648.





